8 800 700 88 88Звонок бесплатный
Доставим завтрав любую из 321 аптеки в Ставрополь
Срок хранения заказа ~ 5 дней
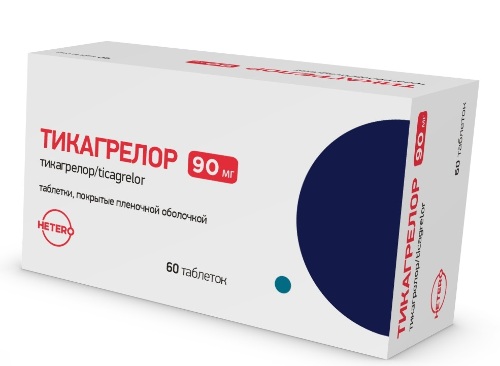
Брилинта в Ставрополе
- Купить Брилинта в Ставрополе в Apteka.ru.
- Цена на Брилинта от 2939.60 руб. в Ставрополе.
- Доставка препарата Брилинта в 322 аптеки.
- Брилинта 60 мг 168 шт. таблетки, покрытые пленочной оболочкойАстраЗенека Индастриз ОООтаблетки, покрытые пленочной оболочкойДозировка 60 мг168 шт в уп.Доставим в аптеку завтраВ наличииЦена:8 695.50₽
- Брилинта 90 мг 56 шт. таблетки, покрытые пленочной оболочкойАстраЗенека Индастриз ОООтаблетки, покрытые пленочной оболочкойДозировка 90 мг56 шт в уп.Доставим в аптеку завтраВ наличииЦена:5 013.70₽
- Брилинта 60 мг 56 шт. таблетки, покрытые пленочной оболочкойАстраЗенека Индастриз ОООтаблетки, покрытые пленочной оболочкойДозировка 60 мг56 шт в уп.Доставим в аптеку завтраВ наличииЦена:2 939.60₽
- Брилинта 90 мг 168 шт. таблетки, покрытые пленочной оболочкойАстраЗенека Индастриз ОООтаблетки, покрытые пленочной оболочкойДозировка 90 мг168 шт в уп.Доставим в аптеку завтраВ наличииЦена:14 677.10₽
Отзывы
- Брилинта 90 мг 56 шт. таблетки, покрытые пленочной оболочкойТовар куплен на Apteka.ruНадеюсь не подделка
- Брилинта 90 мг 56 шт. таблетки, покрытые пленочной оболочкойТовар куплен на Apteka.ruотличные таблетки
- Брилинта 90 мг 56 шт. таблетки, покрытые пленочной оболочкойТовар куплен на Apteka.ruПристо волшебница!!!!!!!!!!?
- Брилинта 90 мг 56 шт. таблетки, покрытые пленочной оболочкойТовар куплен на Apteka.ruПила год после ОКС и стентирования. Рестеноза не было, все хорошо. Стент прижился. Хороший препарат.
- Брилинта 90 мг 56 шт. таблетки, покрытые пленочной оболочкойТовар куплен на Apteka.ruЭффективный препарат
- Брилинта 90 мг 56 шт. таблетки, покрытые пленочной оболочкойТовар куплен на Apteka.ruХорошее лекарство
Брилинта Инструкция по применению
Беречь от детей
Антиагрегантное средство
Производитель
Астра Зенека АБ
Страна происхождения
Швеция
Лекарственная форма
Круглые, двояковыпуклые таблетки, покрытые плёночной оболочкой жёлтого цвета, с гравировкой 90 / Т на одной стороне.
Описание лекарственной формы
Таблетки, покрытые плёночной оболочкой по 90 мг - 168 шт в уп.
Состав
На 1 таблетку:
Активное вещество: тикагрелор 90 мг;
Вспомогательные вещества: маннитол 126 мг, кальция гидрофосфат 63 мг, карбоксиметилкрахмал натрия 9 мг, гипролоза 9 мг, магния стеарат 3 мг;
в составе пленочной оболочки таблетки: гипромеллоза 2910 5,6 мг, титана диоксид Е 171 1,7 мг, тальк 1,0 мг, макрогол 400 0,6 мг, краситель железа оксид жёлтый Е 172 0,1 мг.
Особые условия
Риск развития кровотечения
При назначении препарата Брилинта® следует оценить соотношение пользы от профилактики атеротромботических событий и риска у пациентов с повышенным риском развития кровотечений.
При наличии клинических показаний Брилинта® должна использоваться с осторожностью в следующих группах пациентов:
- Предрасположенность пациентов к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением). Применение препарата Брилинта® противопоказано у пациентов с активным патологическим кровотечением, внутричерепным кровоизлиянием в анамнезе, умеренной или тяжелой печеночной недостаточностью.
- Сопутствующее применение препаратов, которые могут повысить риск развития кровотечения (например, нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики, принимаемые в течение 24 часов до приема препарата Брилинта®).
В исследовании с участием здоровых добровольцев трансфузия тромбоцитов не приводила к прекращению антитромбоцитарного эффекта препарата Брилинта® и, вероятно, не окажет клинического эффекта у пациентов с кровотечением. Так как при сопутствующем применении препарата Брилинта® и десмопрессина не уменьшалось стандартизированное время кровотечения, то маловероятно, что десмопрессин будет эффективно купировать кровотечение (см. раздел "Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия"). Антифибринолитическая терапия (аминокапроновая кислота или транексамовая кислота) и/или рекомбинантный фактор VIIa могут усиливать гемостаз. После установления причины кровотечения и его купирования можно возобновить терапию препаратом Брилинта®.
Хирургические операции
Перед запланированной операцией или началом приема новых препаратов пациенту следует проинформировать врача о том, что он принимает препарат Брилинта®.
В исследовании PLATO у пациентов, подвергавшихся АКШ, при применении препарата Брилинта® было больше кровотечений в сравнении с клопидогрелом при прекращении терапии за один день до хирургического вмешательства, но частота развития больших кровотечений в случае отмены терапии за 2 или более дней до хирургического вмешательства была сходной в группах тикагрелора и клопидогрела (см. раздел "Побочное действие"). Если пациент подвергается плановой операции и не желателен антитромботический эффект, то терапию препаратом Брилинта® следует прекратить за 7 дней до операции (см. раздел "Фармакологические свойства").
Пациенты с предшествующим ишемическим инсультом
Пациенты с ОКС (острый коронарный синдром) с предшествующим ишемическим инсультом могут принимать препарат Брилинта® до 12 месяцев (исследование PLATO).
В исследование PEGASUS не были включены пациенты с инфарктом миокарда в анамнезе с предшествующим ишемическим инсультом. Поэтому при отсутствии данных следует с осторожностью проводить терапию длительностью более 1 года.
Пациенты с печеночной недостаточностью
Применение препарата Брилинта® противопоказано у пациентов с печеночной недостаточностью тяжелой степени (см. разделы "Противопоказания" и "Способ применения и дозы"). Следует соблюдать осторожность у пациентов с печеночной недостаточностью средней степени тяжести, учитывая ограниченный опыт применения препарата у пациентов этой группы (см. разделы "Фармакокинетика" и "Способ применения и дозы")
Пациенты с риском развития брадикардии
В связи с выявлением в ранее проведенном клиническом исследовании, в основном, бессимптомных желудочковых пауз, пациенты с повышенным риском развития брадикардии (например, пациенты без кардиостимулятора, у которых диагностирован синдром слабости синусового узла, атриовентрикулярная блокада сердца 2-ой или 3-ей степени или обморок, связанный с брадикардией) не были включены в основное исследование для оценки безопасности и эффективности препарата Брилинта®. Поэтому, в связи с ограниченным клиническим опытом применения препарата у этих пациентов, рекомендуется с осторожностью назначать им препарат Брилинта® (см. раздел "Фармакологические свойства").
Также следует соблюдать осторожность при совместном применении препарата Брилинта® с препаратами, способными вызвать брадикардию. Однако в исследовании PLATO не отмечалось клинически значимых побочных эффектов при совместном применении с одним или более препаратами, которые могут вызвать брадикардию (например, 96% пациентов одновременно принимали бета-адреноблокаторы, 33% - блокаторы кальциевых каналов, включая дилтиазем и верапамил, и 4% - дигоксин) (см. раздел "Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия"). В ходе под-исследования с использованием суточного мониторирования ЭКГ по Холтеру в группе тикагрелора по сравнению с клопидогрелом больше пациентов в острой фазе ОКС имели желудочковые паузы ? 3 секунд. Повышение числа желудочковых пауз, зарегистрированных с помощью суточного мониторирования по Холтеру, на фоне приема тикагрелора отмечалось чаще у пациентов с хронической сердечной недостаточностью по сравнению с общей популяцией в острой фазе ОКС, но не в первый месяц терапии и не но сравнению с клопидогрелом. Паузы у этих пациентов не сопровождались последующими нежелательными клиническими последствиями (обмороки и установка кардиостимулятора).
Одышка
Сообщалось о развитии одышки у пациентов, принимавших препарат Брилинта®. Одышка при применении препарата Брилинта® обычно слабая или умеренная по своей интенсивности, часто проходит по мере продолжения терапии препаратом. Пациенты с бронхиальной астмой/ХОБЛ могут иметь повышенный абсолютный риск одышки на приеме препарата Брилинта® (см. раздел "Побочное действие"). У пациентов с бронхиальной астмой/ХОБЛ тикагрелор должен использоваться с осторожностью. Механизм одышки на приеме тикагрелора не выяснен. Если у пациента развился новый эпизод одышки, сохраняется или усилилась одышка во время применения препарата Брилинта®, то необходимо провести полноценное обследование, и в случае непереносимости, прием препарата следует прекратить.
Повышение концентрации креатинина
На фоне терапии препаратом Брилинта® концентрация креатинина может увеличиться (см. раздел "Побочное действие"). Механизм этого эффекта не известен. Оценку почечной функции необходимо производить через месяц от начала приема препарата, а в последующем в соответствии с рутинной клинической практикой, обращая особое внимание на пациентов в возрасте 75 лет и старше, пациентов с умеренной или тяжелой почечной недостаточностью и получающих терапию антагонистами рецепторов ангиотензина.
Повышение концентрации мочевой кислоты
На фоне терапии препаратом Брилинта® концентрация мочевой кислоты может повышаться (см. раздел "Побочное действие"). Необходимо соблюдать осторожность у пациентов с гиперурикемией или подагрическим артритом в анамнезе. В качестве превентивной меры следует избегать применения тикагрелора у пациентов с гиперурикемической нефропатией.
Другие
На основании наблюдаемого в исследовании PLATO связи между поддерживающей дозой АСК и эффективностью тикагрелора по сравнению с клопидогрелом, совместное применение высокой поддерживающей дозы АСК (более 300 мг) и препарата Брилинта® не рекомендуется (см. разделы "Фармакологические свойства", "С осторожностью").
Совместное применение препарата Брилинта® с мощными ингибиторами CYP3A4 (например, кетоконазол, кларитромицин, нефазодон, ритонавир и атазанавир) противопоказано (см. раздел "Противопоказания"), так как оно может привести к значительному повышению экспозиции препарата Брилинта® (см. раздел "Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия ").
Совместное применение препарата Брилинта® с мощными индукторами CYP3A4 (например, рифампицин, фенитоин, карбамазепин и фенобарбитал) не рекомендуется, так как их совместный прием может снижать экспозицию и эффективность тикагрелора (см. раздел "Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия").
Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд и алкалоиды спорыньи) не рекомендовано, так как тикагрелор может увеличить экспозицию этих препаратов. Совместное применение препарата Брилинта® с симвастатином или ловастатином в дозе более 40 мг не рекомендуется (см. раздел "Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия").
При совместном применении дигоксина и препарата Брилинта® рекомендован тщательный клинический и лабораторный мониторинг (частоты сердечных сокращений, и при наличии клинических показаний также ЭКГ и концентрации дигоксина в крови).
Нет данных о совместном применении тикагрелора с мощными ингибиторами гликопротеина Р (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы "С осторожностью", "Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия").
Прекращение терапии
Досрочная отмена любой антиагрегантной терапии, включая препарат Брилинта®, может повысить риск сердечно-сосудистой смерти или инфаркта миокарда в результате основного заболевания. Необходимо избегать преждевременного прекращения приема препарата.
Влияние препарата на способность к управлению транспортными средствами и другими механизмами:
Не проводилось исследований влияния препарата Брилинта® на способность к вождению автотранспорта и управлению механизмами. Брилинта® не влияет или в незначительной степени влияет на способность управлять транспортом и механизмами. Во время терапии острого коронарного синдрома сообщалось о головокружении и спутанности сознания. В случае развития данных явлений пациентам следует соблюдать осторожность при управлении автомобилем и другими механизмами.
Лекарственное взаимодействие
Воздействие других лекарственных препаратов на препарат Брилинта®
Лекарственные препараты, метаболизируемые изоферментом CYP3A4
Ингибиторы CYP3A4
- Мощные ингибиторы CYP3A4: совместное применение кетоконазола с тикагрелором увеличивает Сmах и AUC тикагрелора в 2,4 и 7,3 раза, соответственно. Сmах и AUC активного метаболита понижается на 89% и 56%, соответственно. Другие мощные ингибиторы CYP3A4 (кларитромицин, нефазодон, ритонавир и атазанавир) будут оказывать такие же эффекты, поэтому их совместное применение с препаратом Брилинта® противопоказано (см. разделы "Противопоказания", "Особые указания").
- Умеренные ингибиторы CYP3A4: совместное применение дилтиазема с тикагрелором увеличивает Сmах тикагрелора на 69%, a AUC в 2,7 раз, и снижает Сmах активного метаболита на 38%, a AUC не меняется. Тикагрелор не влияет на плазменные концентрации дилтиазема. Другие умеренные ингибиторы CYP3A4 (например, ампренавир, апрепитант, эритромицин, флуконазол) можно назначать одновременно с препаратом Брилинта®.
Циклоспорин (ингибитор P-gp и CYP3A4)
Совместное применение циклоспорина (600 мг) с тикагрелором увеличивает Сmах и AUC тикагрелора в 2,3 и 2,8 раз, соответственно. При этом отмечается увеличение AUC активного метаболита на 32% и снижение Сmах на 15%. Тикагрелор не влияет на плазменную концентрацию циклоспорина.
Индукторы CYP3A4
Совместное применение рифампицина с тикагрелором снижает Сmах и AUC тикагрелора на 73% и 86%, соответственно. Сmах активного метаболита не меняется, a AUC понижается на 46%. Другие индукторы CYP3A4 (например, фенитоин, карбамазепин и фенобарбитал), по-видимому, будут снижать экспозицию препарата Брилинта®. Мощные индукторы CYP3A4 могут уменьшать экспозицию и эффективность препарата Брилинта®.
Другие
По результатам фармакологических исследований взаимодействия, сопутствующее применение тикагрелора с гепарином, эноксапарином и АСК или десмопрессином не влияет на фармакокинетику тикагрелора, его активного метаболита и АДФ-зависимую агрегацию тромбоцитов. В случае наличия клинических показаний к назначению препаратов, влияющих на гемостаз, они должны использоваться с осторожностью в комбинации с препаратом Брилинта® (см. раздел "С осторожностью").
Нет данных о совместном применении препарата Брилинта® с мощными ингибиторами гликопротеина Р (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы "С осторожностью", "Особые указания").
Влияние препарата Брилинта® на другие лекарственные средства
Лекарственные препараты, метаболизируемые изоферментом CYP3A4
- Симвастатин: сопутствующее применение тикагрелора и симвастатина повышает Сmах и AUC симвастатина на 81% и 56%, соответственно, и увеличивает Сmах и AUC симвастатиновой кислоты на 64% и 52%, соответственно, при этом, в некоторых случаях эти показатели повышаются в 2-3 раза. Совместное применение симвастатина в дозе выше 40 мг/сут. с тикагрелором может приводить к развитию побочных эффектов симвастатина, и необходимо оценить соотношение потенциального риска и пользы. Не рекомендуется совместное применение препарата Брилинта® с симвастатином и ловастатином в дозе свыше 40 мг.
- Аторвастатин: сопутствующее применение аторвастатина и тикагрелора повышает Сmах и AUC метаболитов аторвастатиновой кислоты на 23% и 36%, соответственно. Подобное увеличение значений Сmах и AUC наблюдается для всех метаболитов аторвастатиновой кислоты. Эти изменения признаны клинически не значимыми.
- Сходные эффекты со статинами, метаболизирующимися CYP3A4, не могут быть исключены. В исследовании PLATO пациенты, получавшие тикагрелор, принимали различные статины при отсутствии каких-либо опасений относительно безопасности у 93% пациентов, принимавших эту группу препаратов.
Тикагрелор - слабый ингибитор CYP3A4. Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд или алкалоиды спорыньи) не рекомендуется, так как тикагрелор может увеличивать экспозицию этих препаратов.
Лекарственные препараты, метаболизируемые изоферментом CYP2C9
Сопутствующее применение тикагрелора и толбутамида не меняло плазменные концентрации ни одного из этих препаратов, что говорит о том, что тикагрелор не является ингибитором изофермента CYP2C9, и, маловероятно, что он влияет на CYP2C9-опосредованный метаболизм препаратов, подобных варфарину и толбутамиду.
Оральные контрацептивы
Совместное применение тикагрелора, левоноргестрела и этинилэстрадиола увеличивает экспозицию этинилэстрадиола примерно на 20%, но не влияет на фармакокинетику левоноргестрела. Не ожидается клинически значимого воздействия на эффективность контрацепции при одновременном применении левоноргестрела, этинилэстрадиола и препарата Брилинта®.
Субстрат P-gp (включая дигоксин и циклоспорин)
Сопутствующее применение дигоксина с тикагрелором повышает Сmах и AUC дигоксина на 75% и 28%, соответственно. При совместном приеме с тикагрелором среднее значение самой низкой концентрации дигоксина увеличивалось на 30%, в некоторых индивидуальных случаях в два раза. Сmах и AUC тикагрелора при применении дигоксина не менялись. Поэтому рекомендуется проводить соответствующий клинический и/или лабораторный мониторинг при одновременном применении препарата Брилинта® и P-gp-зависимых препаратов с узким терапевтическим индексом, наподобие дигоксина и циклоспорина.
Лекарственные препараты, способные вызвать брадикардию
При совместном применении препарата Брилинта® с препаратами, способными вызвать брадикардию, должна соблюдаться осторожность. Однако в исследовании PLATO не наблюдалось клинически значимых нежелательных явлений при совместном применении с одним или более препаратами, способными вызвать брадикардию (например, 96% пациентов одновременно принимали бета-адреноблокаторы, 33% - блокаторы "медленных" кальциевых каналов, включая дилтиазем и верапамил, и 4% - дигоксин).
Другая сопутствующая терапия
В клинических исследованиях препарат Брилинта® преимущественно назначался совместно с АСК, ингибиторами протонной помпы, статинами, бета-адреноблокаторами, ингибиторами ангиотензинпревращающего фермента и антагонистами рецепторов ангиотензина в рамках длительного приема, а также с гепарином, низкомолекулярными гепаринами, ингибиторами гликопротеиновых IIb/IIIa рецепторов для внутривенного введения в рамках краткосрочной терапии. По результатам этих исследований не выявлено клинически значимых нежелательных взаимодействий.
Совместное применение препарата Брилинта® с гепарином, эноксапарином или десмопрессином не оказывало влияние на активированное частичное тромбопластиновое время (АЧТВ), активированное время свертывания (АВС) и исследование фактора Ха, однако вследствие потенциального фармакодинамического взаимодействия, требуется соблюдать осторожность при совместном применении с препаратами, влияющими на гемостаз.
В связи с сообщениями о подкожных кровоизлияниях на фоне селективных ингибиторов обратного захвата серотонина (например, пароксетин, сертралин и циталопрам), рекомендуется соблюдать осторожность при их совместном приеме с препаратом Брилинта®.
При ежедневном употреблении больших объемов грейпфрутового сока (по 200 мл 3 раза в день) было отмечено 2-кратное увеличение экспозиции тикагрелора. Ожидается, что такое увеличение экспозиции тикагрелора не имеет клинического значения для большинства пациентов.
Фармакокинетика
Тикагрелор демонстрирует линейную фармакокинетику, и экспозиция тикагрелора и активного метаболита (AR-C124910XX) примерно пропорциональна дозе вплоть до 1260 мг.
Абсорбция
Тикагрелор быстро абсорбируется со средней tmax примерно 1,5 часа. Формирование основного циркулирующего в крови метаболита AR-C124910XX (также активного) из тикагрелора происходит быстро со средней tmax примерно 2,5 часа. После приема натощак тикагрелора в дозе 90 мг Сmax составляет 529 нг/мл и AUC - 3451 нг*ч/мл.
Средняя абсолютная биодоступность тикагрелора составляет 36%. Прием жирной пищи не влияет на Сmax тикагрелора или AUC активного метаболита, но приводит к повышению на 21% AUC тикагрелора и снижению на 22% Сmax активного метаболита. Эти небольшие изменения имеют минимальную клиническую значимость; поэтому тикагрелор можно назначать вне зависимости от времени приема пищи.
Тикагрелор в виде суспензии измельченных таблеток в питьевой воде, принятой внутрь или введенной в желудок через назогастральный зонд, биоэквивалентен тикагрелору, принятому внутрь в виде таблеток препарата Брилинта® (AUC и Сmax тикагрелора и активного метаболита в диапазоне 80-125%).
В случае приема суспензии первоначальная экспозиция (через 0,5 ч и 1 ч после приема) была выше, чем при приеме тикагрелора в виде таблеток препарата Брилинта®, но в дальнейшем (от 2 до 48 часов) профиль концентраций был практически одинаковым.
Распределение
Объем распределения тикагрелора в равновесном состоянии составляет 87,5 л. Тикагрелор и активный метаболит активно связываются с белками плазмы крови (> 99%).
Метаболизм
CYP3A4 является основным изоферментом, отвечающим за метаболизм тикагрелора и формирование активного метаболита, и их взаимодействия с другими субстратами CYP3A варьируют от активации до ингибирования. Тикагрелор и активный метаболит являются слабыми ингибиторами гликопротеина Р (P-gp).
Основным метаболитом тикагрелора является AR-C124910XX, который также активен, что подтверждается результатами оценки связывания с P2Y12-рецептором АДФ тромбоцитов in vitro. Системная экспозиция активного метаболита составляет примерно 30-40% от экспозиции тикагрелора.
Экскреция
Основной путь выведения тикагрелора - через печеночный метаболизм. При введении меченного изотопом тикагрелора в среднем примерно 57,8% радиоактивности выделяется с фекалиями, 26,5% с мочой. Выведение тикагрелора и активного метаболита с мочой составляет менее 1% дозы. В основном активный метаболит выводится с желчью. Средний период полувыведения тикагрелора и активного метаболита составлял 7 и 8,5 часов, соответственно.
Особые популяции пациентов
Пожилые пациенты
У пожилых пациентов (в возрасте от 75 лет и старше) отмечена более высокая экспозиция тикагрелора (Сmax и AUC примерно на 25% выше) и активного метаболита по сравнению с молодыми пациентами. Эти различия не считаются клинически значимыми (см. раздел "Способ применения и дозы").
Дети
Нет данных по применению тикагрелора у детей.
Пол
У женщин отмечена более высокая экспозиция тикагрелора и активного метаболита по сравнению с мужчинами. Эти различия не считаются клинически значимыми.
Этнические группы
Средняя биодоступность препарата у пациентов-азиатов на 39% выше, чем у европеоидов. Биодоступность препарата Брилинта® на 18% ниже у пациентов негроидной расы по сравнению с пациентами европеоидной расы.
Почечная недостаточность
Экспозиция тикагрелора примерно на 20% ниже, а его активного метаболита примерно на 17% выше у пациентов с тяжелой почечной недостаточностью (клиренс креатинина < 30 мл/мин) по сравнению с пациентами с нормальной функцией почек (см. раздел "Способ применения и дозы").
Печеночная недостаточность
Сmax и AUC тикагрелора были на 12% и 23% выше у пациентов с печеночной недостаточностью легкой степени по сравнению со здоровыми добровольцами. Не проводились исследования тикагрелора у пациентов с печеночной недостаточностью тяжелой степени, и его использование у этих пациентов противопоказано (см. разделы "Способ применения и дозы" и "Противопоказания"). Фармакокинетические параметры препарата Брилинта® у пациентов с печеночной недостаточностью средней степени тяжести не изучены (см. разделы "Способ применения и дозы" и "Особые указания").
Показания
Брилинта®, применяемая одновременно с ацетилсалициловой кислотой, показана для профилактики атеротромботических событий у пациентов с острым коронарным синдромом (нестабильной стенокардией, инфарктом миокарда без подъема сегмента ST или инфарктом миокарда с подъемом сегмента ST [STEMI]), включая пациентов, получавших лекарственную терапию, и пациентов, подвергнутых чрескожному коронарному вмешательству (ЧКВ) или аортокоронарному шунтированию (АКШ).
Противопоказания
- Повышенная чувствительность к тикагрелору или любому из компонентов препарата;
- активное патологическое кровотечение;
- внутричерепное кровоизлияние в анамнезе;
- печеночная недостаточность тяжелой степени;
- совместное применение тикагрелора с мощными ингибиторами CYP3A4 (например, кетоконазолом, кларитромицином, нефазодоном, ритонавиром и атазанавиром);
- детский возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности применения у данной группы пациентов).
С осторожностью:
Предрасположенность к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением) (см. раздел "Особые указания").
Сопутствующая терапия препаратами, повышающими риск кровотечений (т.е. нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики) в течение 24 часов до приема препарата Брилинта®.
Пациенты с повышенным риском развития брадикард
Передозировка
Тикагрелор хорошо переносится в однократной дозе препарата до 900 мг. В единственном исследовании с увеличением дозы неблагоприятное воздействие на желудочно-кишечный тракт было дозолимитирующим. Другими клинически значимыми нежелательными явлениями, которые могли наблюдаться при передозировке, были одышка и желудочковые паузы. В случае передозировки рекомендуется осуществлять наблюдение на предмет этих нежелательных явлений и проводить мониторирование ЭКГ.
Брилинта® не выводится при гемодиализе (см. раздел «Особые указания»), антидот не известен. При передозировке следует проводить симптоматическую терапию в соответствии с локальными стандартами. В связи с ингибированием тромбоцитов увеличение продолжительности кровотечения является предполагаемым фармакологическим действием передозировки препаратом Брилинта®, поэтому при развитии кровотечения необходимо проводить соответствующие поддерживающие мероприятия.
Побочные действия
По данным исследования PLATO самыми частыми отмечавшимися нежелательными явлениями у пациентов, принимавших тикагрелор, были одышка, ушибы и носовые кровотечения.
Нежелательные реакции классифицированы по частоте развития и классу системы органов. Частота развития нежелательных реакций определяется с использованием следующих условных обозначений: очень часто (больше или равно1/10), часто (больше или равно1/100, меньше1/10), нечасто (больше или равно1/1000, меньше1/100), редко (больше или равно1/10000, меньше1/1000).
Нежелательные лекарственные реакции по частоте развития и классу системы органов
Метаболизм и питание
Редко
Гиперурикемия (гиперурикемия, повышение концентрации мочевой кислоты в крови; смотрите раздел «Отклонения в значениях лабораторных показателей» ниже)
Нервная система
Нечасто
Внутричерепное кровоизлияние (кровоизлияние в мозг, внутричерепное кровоизлияние, геморрагический инсульт), головная боль,
головокружение
Редко
Парестезия,спутанность сознания
Органы зрения
Нечасто
Кровоизлияния (интраокулярные, конъюнктивальные, ретинальные)
Органы слуха
Редко
Кровоизлияние в ухо, вертиго
Дыхательная система
Часто
Одышка (одышка, одышка при нагрузке, одышка в покое, ночная одышка), носовое кровотечение
Нечасто
Кровохарканье
Пищеварительная система
Часто
Желудочно-кишечные кровотечения (желудочно-кишечное кровотечение, ректальное кровотечение, кишечное кровотечение, мелена, положительный анализ на скрытую кровь)
Нечасто
Рвота с кровью, кровотечения из язвы ЖКТ (кровотечение из язвы ЖКТ, кровотечение из язвы желудка, кровотечение из язвы двенадцатиперстной кишки, кровотечение из пептической язвы), геморроидальные кровотечения, гастрит, кровотечения в ротовой полости (включая гингивальные кровотечения), рвота, диарея, абдоминальная боль, тошнота, диспепсия)
Редко
Ретроперитонеальное кровотечение, запор
Кожа и подкожные ткани
Часто
Подкожные или кожные геморрагии (подкожная гематома, кожные и подкожные геморрагии, петехии), синяки (ушиб, гематома, экхимоз, повышенная тенденция к синякам, травматическая гематома )
Нечасто
Сыпь, зуд
Опорно-двигательная система
Редко
Гемартроз (у пациентов, принимавших тикагрелор в исследовании PLATO (n=9235), случаев гемартроза отмечено не было. Частота гемартроза была рассчитана с использованием верхнего предела 95% ДИ для ожидаемой частоты (по формуле 3/Х, где Х – количество пациентов, получавших тикагрелор, т.е. 9235). Предполагаемая частота гемартроза составляет 3/9235, что соответствует частоте «редко»)
Мочевыводящая система
Нечасто
Кровотечение
из мочевыводящих путей (гематурия, кровотечение из мочевыводящих путей )
Репродуктивная система
Нечасто
Вагинальные кровотечения (включая метроррагии)
Отклонения лабораторных показателей
Редко
Увеличение концентрации креатинина в крови
Прочие
Часто
Кровотечение на месте проведения процедуры (кровотечение из места пункции сосуда, гематома в месте пункции сосуда, кровотечение из места инъекции, кровотечение из места пункции, кровотечение из места катетеризации)
Нечасто
Кровотечение после процедуры
Редко
Кровотечение из раны, травматическое кровотечение
Описание некоторых нежелательных реакций
Кровотечение
В исследовании PLATO использовались следующие определения кровотечения:
-Большое летальное/угрожающее жизни кровотечение: летальное, или внутричерепное кровоизлияние, или кровотечение в полость перикарда с тампонадой сердца; или гиповолемический шок или тяжелая гипотония, вызванные кровотечением и требующие применения вазоконстрикторов или проведения оперативного вмешательства, или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина более, чем на 50 г/л, или требующее трансфузии 4 или более единиц цельной крови или эритроцитов.
-Большое иное кровотечение: вызывающее существенную недееспособность больного (например, внутриглазное кровоизлияние с необратимой потерей зрения), или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина на 30-50 г/л, или требующее трансфузии 2-3 единиц цельной крови или эритроцитов.
-Малое кровотечение: требует медицинского вмешательства для остановки или лечения кровотечения (например, носовое кровотечение, требующее посещения больницы для тампонады носа).
Брилинта® и клопидогрел не различались по частоте больших кровотечений в целом по критериям PLATO (11,6%/год и 11,2%/год, соответственно), летальных/угрожающих жизни кровотечений по критериям PLATO (5,8%/год в обеих группах). Однако частота совокупности больших и малых кровотечений по критериям PLATO была выше в группе тикагрелора (16,1%) по сравнению с клопидогрелом (14,6%, р=0,0084).
Возраст, пол, масса тела, раса, географический регион, сопутствующие заболевания, сопутствующая терапия, анамнез, включая предшествующий инсульт и транзиторную ишемическую атаку, не влияли на частоту больших кровотечений в целом и несвязанных с процедурами по критериям PLATO. Не было выявлено групп с повышенным риском кровотечений.
Кровотечение, связанное с АКШ: В исследовании PLATO у 42% больных из 1584 (12% из когорты), подвергнутых АКШ, развивались большие летальные/ угрожающие жизни больного кровотечения без значимых различий в обеих группах лечения. Летальное кровотечение, связанное с АКШ, отмечалось у 6 пациентов в каждой группе лечения.
Кровотечение, не связанное с АКШ, и кровотечение, не связанное с процедурами: Брилинта® и клопидогрел не отличались по частоте случаев большого летального/ угрожающего жизни кровотечения, не связанного с АКШ по критериям PLATO, но при применении препарата Брилинта® чаще развивались большие кровотечения в целом по определению исследования PLATO (4,5%/год по сравнению с 3,8%/год; р=0,0264). Если удалить случаи развития кровотечений, связанных с АКШ, в группе тикагрелора отмечалось больше кровотечений (3,1%/год), чем в группе клопидогрела (2,3%/год; р=0,0058). Прекращение лечения вследствие кровотечений, не связанных с процедурой, было более частым на фоне тикагрелора (2,9%) по сравнению с клопидогрелом (1,2%, p<0,001).
Внутричерепное кровоизлияние: В группе тикагрелора развивалось больше внутричерепных кровотечений, не связанных с процедурами (n=27 кровотечений у 26 пациентов, 0,3%), чем в группе клопидогрела (n=14 кровотечений, 0,2%), из которых 11 кровотечений на тикагрелоре и 1 на клопидогреле были фатальными. Однако не было значимых различий по общему числу фатальных кровотечений.
Одышка
Нежелательные явления в виде одышки (одышка, одышка в покое, одышка при физической нагрузке, пароксизмальная ночная одышка и ночная одышка) в комбинации развивались у 13,8% больных, получавших препарат Брилинта®, и у
7,8% пациентов, принимавших клопидогрел. Исследователи посчитали, что у 2,2% пациентов из группы тикагрелора одышка была связана с терапией. Большинство случаев одышки были слабыми или умеренными по своей интенсивности и представляли собой однократные эпизоды сразу после начала терапии.
Примерно 30% от всех случаев одышки разрешились в течение 7 дней. Чаще одышка развивалась у пожилых больных, у пациентов с застойной сердечной недостаточностью, ХОБЛ или бронхиальной астмой в начале исследования. 0,9% пациентов прекращали прием препарата Брилинта® из-за одышки. Одышка не была связана с развитием нового или ухудшением имеющегося заболевания сердца или легких (см. раздел «Особые указания»).
Препарат Брилинта® не влияет на показатели функции внешнего дыхания.
Отклонения в значениях лабораторных показателей
Сывороточная концентрация креатинина повышалась более, чем на 30% у 25,5% пациентов и больше, чем на 50% у 8,3% пациентов, получающих препарат Брилинта®. Повышение креатинина более, чем на 50%, чаще встречалось у пациентов старше 75 лет, у пациентов с тяжелой почечной недостаточностью при включении в исследование и у пациентов, получающих терапию антагонистами рецепторов к ангиотензину. Общее число почечных нежелательных явлений составляло 4,9% у пациентов на тикагрелоре, однако исследователи связывали их с приемом препарата в 0,6% случаев.
Сывороточная концентрация мочевой кислоты увеличивалась выше верхней границы нормы у 22% пациентов, получающих препарат Брилинта®. Нежелательные явления, связанные с гиперурикемией, отмечались в 0,5% случаев на тикагрелоре, из них исследователи связывали с приемом тикагрелора 0,05% случаев. Подагрический артрит наблюдался у 0,2% пациентов на тикагрелоре, ни один из этих случаев не был расценен исследователем, как связанный с приемом препарата.
Постмаркетинговое применение
Ниже представлены нежелательные реакции, которые были отмечены при постмаркетинговом применении препарата Брилинта®. Поскольку сообщения получены спонтанно от популяции неустановленного размера, не всегда возможно достоверно оценить частоту развития.
Нарушения со стороны иммунной системы: реакции повышенной чувствительности, включая ангионевротический отек (см. раздел «Противопоказания»).
Список литературы:
1. Государственный реестр лекарственных средств ;
2. Анатомо-терапевтическо-химическая классификация (ATX);
3. Официальная инструкция от производителя.
Аналоги Брилинта в Ставрополе
Тикагрелор 60 мг 60 шт. таблетки, покрытые пленочной оболочкойМАКИЗ-ФАРМА ООО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
60 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
1 770₽
Когавант 90 мг 56 шт. таблетки, покрытые пленочной оболочкойGEDEON RICHTER
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
56 шт в уп.
Нет в наличии
Катилорикс 90 мг 60 шт. таблетки, покрытые пленочной оболочкойИзварино Фарма ООО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
60 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
3 813.40₽
Катилорикс 60 мг 60 шт. таблетки, покрытые пленочной оболочкойИзварино Фарма ООО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
60 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 037.90₽
Грелорта 60 мг 60 шт. таблетки, покрытые пленочной оболочкойАкрихин ХФК АО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
60 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
1 632.30₽
Тикагрелор 60 мг 56 шт. таблетки, покрытые пленочной оболочкойОЗОН ООО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
1 323.50₽
Тикагрелор 90 мг 56 шт. таблетки, покрытые пленочной оболочкойОЗОН ООО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 245.80₽
Тикагрелор 90 мг 168 шт. таблетки, покрытые пленочной оболочкойОЗОН ООО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
168 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
6 692.20₽
Катилорикс 60 мг 170 шт. таблетки, покрытые пленочной оболочкойИзварино Фарма ООО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
170 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
5 669.40₽
Тикагрелор медисорб 90 мг 56 шт. таблетки, покрытые пленочной оболочкойМедисорб АО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
3 368.20₽
Грелорта 90 мг 60 шт. таблетки, покрытые пленочной оболочкойАкрихин ХФК АО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
60 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 152.80₽
Тикагрелор-вертекс 90 мг 168 шт. блистер таблетки, покрытые пленочной оболочкойВертекс АО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
168 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
6 959.30₽
Когавант 60 мг 56 шт. таблетки, покрытые пленочной оболочкойGEDEON RICHTER
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 123.30₽
Тикагрелор медисорб 60 мг 56 шт. таблетки, покрытые пленочной оболочкойМедисорб АО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 069.80₽
Тикагрелор 60 мг 168 шт. таблетки, покрытые пленочной оболочкойОЗОН ООО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
168 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
4 004.90₽
Тикагрелор 90 мг 56 шт. таблетки, покрытые пленочной оболочкойАлиум АО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
3 209.20₽
Катилорикс 90 мг 170 шт. таблетки, покрытые пленочной оболочкойИзварино Фарма ООО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
170 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
9 139.10₽
Тикагрелор-вертекс 90 мг 56 шт. блистер таблетки, покрытые пленочной оболочкойВертекс АО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 652.20₽
Тикагрелор 60 мг 56 шт. таблетки, покрытые пленочной оболочкойАлиум АО
таблетки, покрытые пленочной оболочкой
Дозировка 60 мг
56 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 120.60₽
Тикагрелор 90 мг 60 шт. таблетки, покрытые пленочной оболочкойМАКИЗ-ФАРМА ООО
таблетки, покрытые пленочной оболочкой
Дозировка 90 мг
60 шт в уп.
Доставим в аптеку завтра
В наличии
Цена:
2 839₽
Лицензии
Фото
Доставка Брилинта в Ставрополе
Заказывая на Apteka.ru, можно выбрать доставку в удобную для вас аптеку рядом с домом или по дороге на работу.
Все пункты доставки в Ставрополе – 322 аптеки.
- На страницу аптекиОфтальмологическая Аптека. Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Матросова, 65аПН-СБ, 09:00-19:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиООО "Ставропольские городские аптеки10" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Заводская, 5ПН-ПТ, 09:00-18:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Доваторцев, 25, нежилые помещения № 36,37 этаж 1ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. 45 Параллель, 3б в квартале 524, нежилые помещения № 12,13, цокольный этажежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиИП Петросян А.В., Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Серова, 478 аежедневно с 08:00 по 21:00Способы оплаты:Наличные - На страницу аптекиООО *Биолюкс* Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Ленина, 436, нежилые помещения № 58-60,этаж 1ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Ленина, д.410, нежилые помещения №48,50-53,56,62,67,68,72круглосуточноСпособы оплаты:НаличныеБезналичная оплата - На страницу аптекиООО *Социальная Аптека Ставрополь*, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Ленина, д. 415 еежедневно с 07:30 по 20:30Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиООО *Социальная Аптека Ставрополь*, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Мира, д. 280/5ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Тухачевского, 20/1, нежилые помещения №81-86, этаж1круглосуточноСпособы оплаты:НаличныеБезналичная оплата
- На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Гагарина, 2, нежилые помещения № 34-36, этаж 1ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. 50 лет ВЛКСМ, 22, нежилые помещения №20-23, 40 этаж 1ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, Монастырский туп., 2а, этаж 1ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиАптека. Отпуск иммунобиологических препаратов не производится
5г. Ставрополь, ул. Артема, д. 5ПН-ПТ, 09:00-19:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиПЛАНЕТА ЗДОРОВЬЯ
5г. Ставрополь, ул. 50 лет ВЛКСМ, д. 16/4, помещ. 1, часть помещ. №49, этаж 1ежедневно с 09:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиСтавропольские городские аптеки, ООО ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Доваторцев, 9.ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиАНГ Городская Здравница, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, Старомарьевское ш., д.13 часть помещения №1ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека" Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. 60 лет Победы, д. 21, часть помещения № 1, помещения № 14, 16, 17.ежедневно с 08:00 по 19:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Городская аптека", Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Полеводческая, д.1, помещ. 10.ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Аптека Байгера", ООО ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, пр-кт Карла Маркса, д.50/34, Литер "А",помещения № 57. 64-68, 76-80, 87.круглосуточноСпособы оплаты:НаличныеБезналичная оплата
- На страницу аптекиСтавропольские городские аптеки, 5 Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Льва Толстого, д. 3, помещения № 1-5.ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптеки"Эконом Аптека", Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Ленина, дом № 448, помещения № 26.ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплата - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Руставели, дом 69, этаж 1, часть помещения 2ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, 50 лет ВЛКСМ ул, дом № 79, квартал 525, 1 этаж, помещение № 2ежедневно с 08:00 по 21:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Тухачевского, д. 21/2, офис 17ежедневно с 09:00 по 21:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Рогожникова, д. 19/6, помещ. 8, этаж 1, часть помещения № 64ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Доваторцев, д. 46д, помещение 1, этаж 1ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Ленина, д. 385/10, офис 1ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул. Тюльпановая, д. 53ежедневно с 09:00 по 18:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду - На страницу аптекиАптека Апрель, Отпуск ИММУНОБИОЛОГИЧЕСКИХ ПРЕПАРАТОВ в аптеке не производится
5г. Ставрополь, ул Голенева, д. 47, помещ. 4, этаж 1, часть помещения № 15ежедневно с 08:00 по 20:00Способы оплаты:НаличныеБезналичная оплатаОплата по QR-коду